Bakgrunn
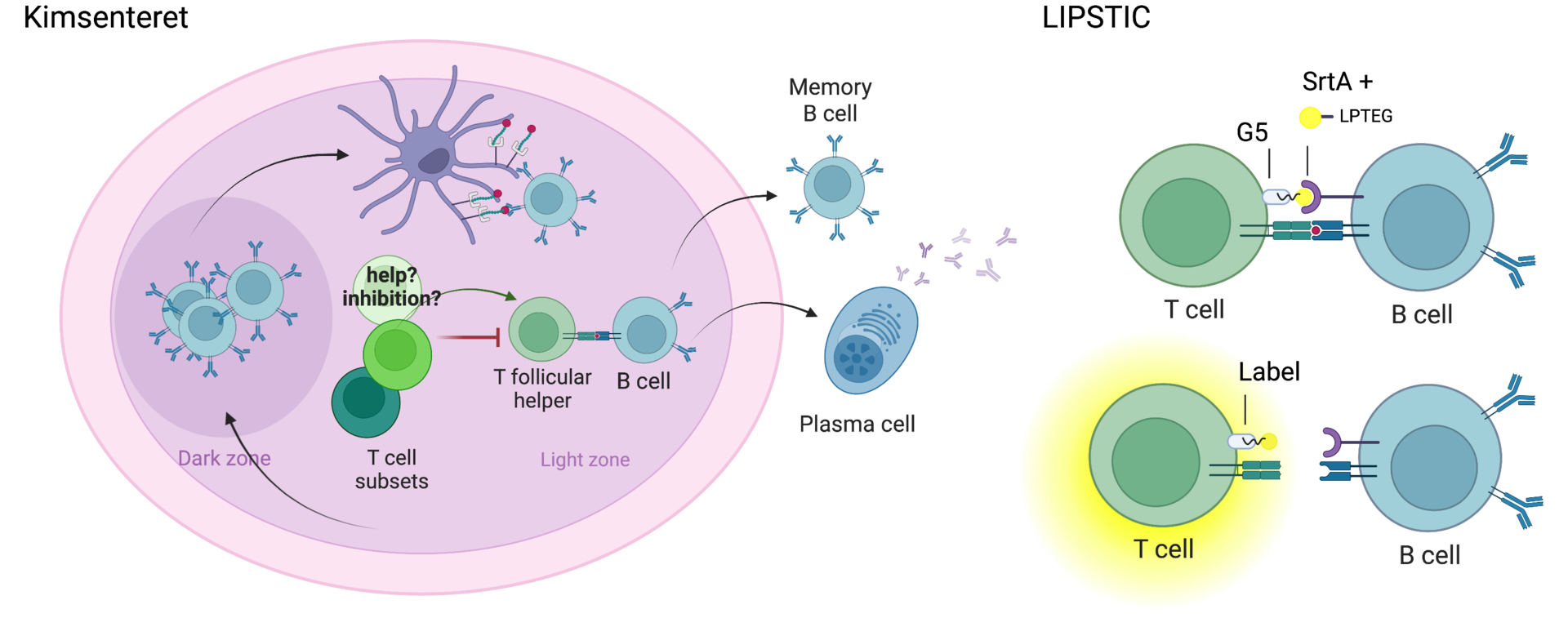
Hvordan kan man lage effektive vaksiner? Hvordan kan man oppnå bredt nøytraliserende antistoffer som effektivt forsvarer mot patogener? Hvordan oppstår antistoffer som angriper kroppens egne komponenter (autoantistoffer)? For å forstå dette må vi forstå hva som driver utviklingen av B-celler. B-cellene i det adaptive immunforsvaret modnes til å bli hukommelsesceller og plasmaceller som produserer beskyttende antistoffer. Dette skjer i lymfeknuter i den såkalte kimsenterreaksjonen. Kimsenterreaksjonen fungerer som en evolusjonsfabrikk der B-cellene hurtig muteres for å oppnå de beste variantene i beskyttelsen mot virus og bakterier. Som drivere og dempere av denne prosessen finner vi T-celler, spesielt T-follikulære hjelpeceller. For at T-follikulære hjelpeceller skal kunne drive seleksjonen av B-celler, må de inngå i antigen-spesifikke interaksjoner der B-cellene presenterer det fremmede antigenet for T-cellene.
Det har nylig blitt avdekket at bildet av hvilke T-celler som driver og demper kimsenterreaksjonen er mer komplekst enn tidligere antatt. Det finnes flere forskjellige underklasser av T-celler i kimsenteret. Vi har vist at T-follikulære hjelpeceller kan begynne å uttrykke en faktor som bidrar til å dempe hele kimsenterreaksjonen. Disse T-cellene endrer fenotype fra å være en driver i kimsenteret til å bli en demper, en regulatorisk T-celle. Vi vil avdekke flere slike undergrupper av T-celler og mekanismene som ligger til grunn for deres drivende eller dempende effekt. Dette vil vi gjøre på en helt ny og unik måte ved å enzymatisk merke cellene som interagerer med hverandre. I tillegg vil vi bruke optogenetisk merking av kimsenteret for å sortere ut og analysere alle T-celler, uavhengig av hvilke markører de uttrykker.
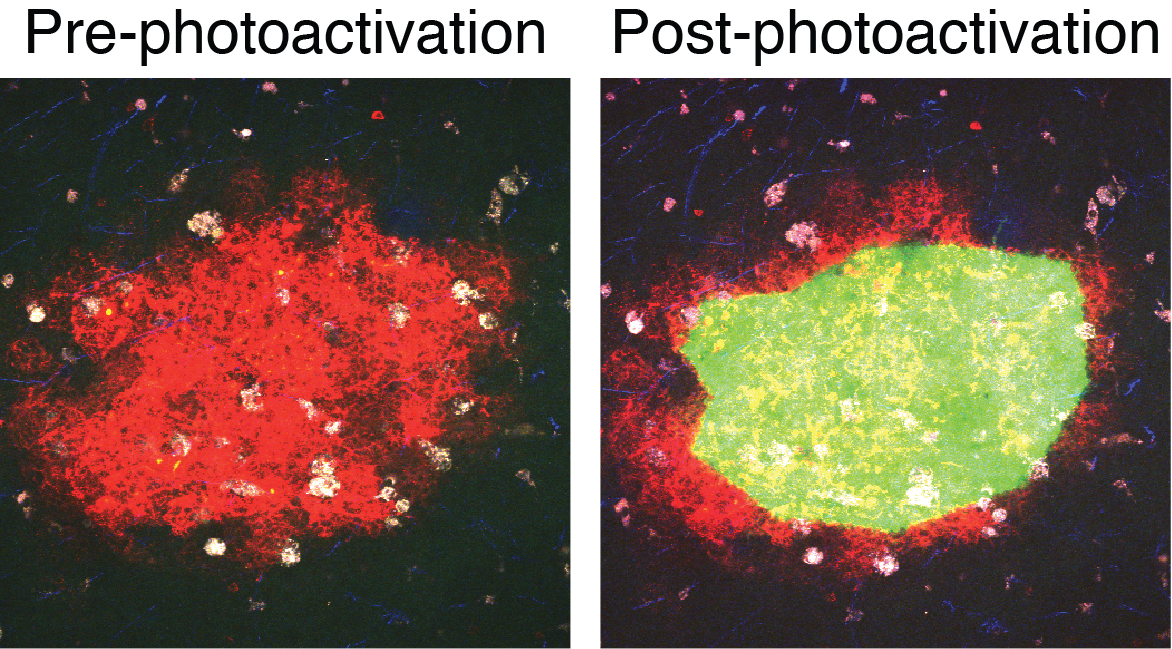
LIPSTIC (Labelling Immune Partnerships by SorTagging Intercellular Contacts) bruker transpeptidasen SortaseA (SrtA) fra Staphylococcus aureus for å overføre et peptidsubstrat med motivet LPETG til den N-terminale pentaglycinen G5. På denne måten blir den G5+ cellen som inngår i en interaksjon med den SrtA+ cellen merket for nedstrømsanalyse (se Figur. 1). Ved å bruke transgene mus som uttrykker fotoaktivert grønt fluorescerende protein (GFP), kan vi merke hele kimsenteret ved å bestråle det med en bestemt bølgelengde av laser (820 nm). Dette betyr at vi kan sortere ut alle celler i ett eller flere kimsenter, uavhengig av hvilke markører de uttrykker (se Figur 2).
Problemstillinger
- Hvilke undergrupper av T-celler driver eller demper kimsenteret på forskjellige tidspunkt i reaksjonen.
- Hva er mekanismen for drivkraften eller den regulatoriske effekten til de forskjellige undergruppene av T-celler.
- Hvordan påvirker de forskjellige undergruppene av T-celler fenotypen til B cellene som blir selektert i kimsenteret.
- Kan vi modulere B celle fenotypen ved å modulere de forskjellige subklassene av T celler?
Mål og metode
- Grunnleggende karakterisering av når i kimsenter reaksjonen vi har best merking av T-celler i vårt LIPSTIC-system.
- Merke og sortere ut T-celler for nedstrøms enkeltcelle TCR-sekvensering eller enkeltcelle RNA sekvensering. Ifra dette, finne nye undergrupper og markører, nye mekanismer for kimsenter/B-celle regulering.
- Fotoaktivering av kimsenter med LIPSTIC for å inkludere alle T celler i kimsenteret.
- Oppfølging in vitro/in vivo med funksjonelle assay, eventuelle knock-out/knock-in musemodeller.
Studentens arbeidsoppgaver
- Kryssing av mus
- Karakterisering av systemet for å finne optimale tidspunkter for analyse og optimale immuniseringer. Flow Cytometri.
- Merke celler og utføre enkeltcelle sortering av T celler for enten TCR enkeltcelle sekvensering eller RNA sekvensering.
- Fotoaktivering av kimsenter med 2-foton mikroskop.
- Analyse av T-celle reseptor repertoar og analyse and enkeltcelle RNA sekvensering.
- In vitro assay: NFAT hybridom reporter assay for å teste TCR spesifisitet og inhibisjons/proliferasjons assay.
- Design av knock-in/knock-out mus.
Om forskningsmiljøet
Vi har nettopp startet en forskningsgruppe ved Institutt for Immunologi og Transfusjonsmedisin, Avdeling for Klinisk Medisin. Vi jobber med intravital 2-foton mikroskopi og nye musemodeller for å avdekke hvordan T celler driver det adaptive immunforsvaret.