Bakgrunn
Fettvevet anses ikke lenger som et rent lagringsdepot, men er nå anerkjent som et komplekst endokrint organ, dette gjelder også fettvevet som omkranser hjerte, både det epikardiale og perikardiale. Skadelige stimuli mot fettvevet, slik som overvekt, diabetes, røyking og en stillesittende livsstil kan føre til en ugunstig remodelering av fettvevet og en lavgradig inflammasjon med infiltrasjon av leukocytter/makrofager, slik at det blir mer pro-inflammatorisk (Figur 1).
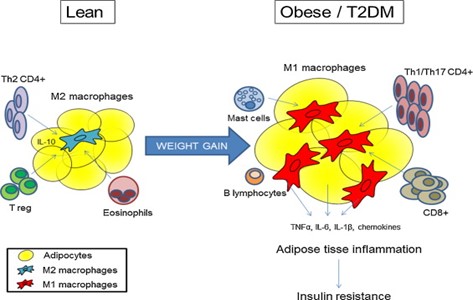
Fettvevet vil nå skille ut adipocytokiner som forverrer inflammasjonen. Ved ugunstig remodelering, vokser adipocyttene i størrelse (hypertrofi). Dette er mulig ved at ekstracellulært matrix (ECM) degraderes ved hjelp av matrix metalloproteinaser (MMPs), spesielt MMP-9. MMP-9 kan induseres av en ekstracellulær matrixmetalloproteinase-induktor (EMMPRIN), og hemmes av tissue inhibitor of metalloproteinase 1 (TIMP-1) (Figur 2)
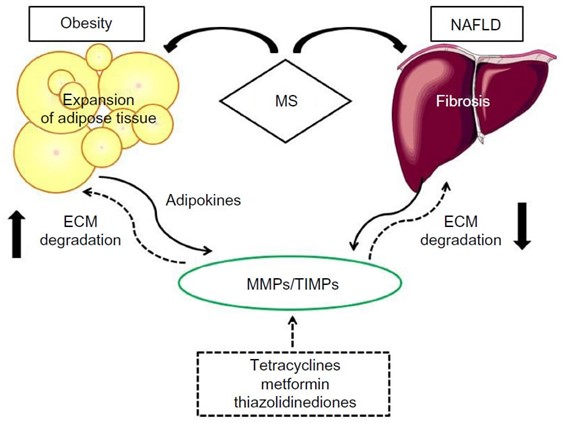
Det epikardiale fettvevet omkranser myokard og får sin blodførsel fra koronararteriene (Figur 3). I tillegg til å være et energi lager for kardiomyocyttene, vil et ugunstig remodelert fettvev sende ut signaler som adipokiner til myokard og koronarteriene via direkte kommunikasjon. Dette vil kunne skade myokardvevet, f.eks ved endret kontraktilitet i kardiomyocyttene, og en muligens akselerert vaskulær aterosklerose.
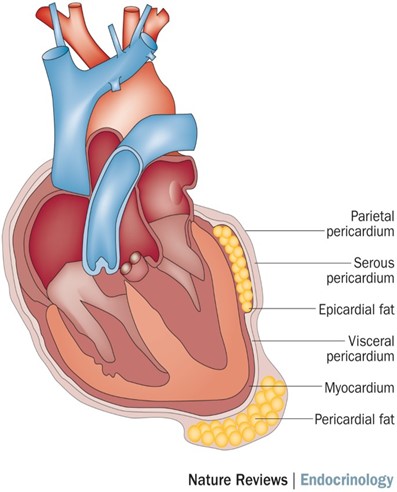
Det perikardiale fettvevet ligger inni og på den eksterne siden av hjerteposen (perikard), og er derfor ikke i direkte kontakt med myokard (Figur 3). Det perikardiale fettvevet får sin blodforsyning fra vaskulaturen i thorax. Ugunstige signaler fra det perikardiale fettvevet vil derfor ikke påvirke myokard direkte, men vil kunne gi en systemisk effekt lignende det man kan forvente å se fra subkutant fettvev.
Vi har tidligere publisert resultater fra denne populasjonen (ATICH studien), hvor en inflammatorisk signalvei er studert, og hvor uttrykk av makrofag differensieringsmarkører og spesifikke cellemarkører ble undersøkt i fettvevet.
Problemstilling
Det er holdepunkter for at det epikardiale og perikardiale fettvevet, som har ulikt opphav (det epikardiale fra splanchnopleurisk mesoderm og det pericardiale fra de mesenkymale stamcellene i thorax), vil remodeleres forskjellig. Vi ønsker derfor å belyse remodeleringsprosessen i de to fettvevsdepotene. I tillegg vil vi se om remodeleringen in det subkutane fettvevet vil reflektere prosessene i de koronare fettdepotene, og om der foreligger ulik remodelering hos pasienter med koronar hjertesykdom i forhold til individer uten kjent koronarsykdom.
- Undersøke genuttrykket av MMP-9, EMMPRIN og TIMP1 i biopsier tatt fra det epikardiale-, perikardiale- og subkutane fettvevet under åpen hjertekirurgi
- Måle sirkulerende konsentrasjoner av MMP-9, EMMPRIN og TIMP1 hos de samme individene
- Resultater fra overnevnte analyser hos hjertepasientene vil bli sammenlignet med prøver tatt fra individer som får skiftet sin aortaklaff. Disse individene inkluderes som kontroller i studien og hadde ved undersøkelse ingen tegn på koronarsykdom.
Mål og metode
- Vi ønsker å belyse remodeleringsprosessen i koronart fettvev, noe som er lite kjent. Til dette vil vi benytte oss av innsamlet materiale i ATICH studien (Adipose Tissue in Coronary Heart disease) utført ved Senter for Klinisk Hjerteforskning ved Hjertemedisinsk avdeling, Oslo universitetssykehus Ullevål i samarbeid med Thoraxkirurgisk avdeling ved Oslo universitetsykehus Ullevål, i perioden 2016-2018. ATICH studien inkluderte 52 pasienter med kjent koronarsykdom henvist til åpen hjertekirurgi (coronary artery bypass grafting - CABG), og 22 individer henvist til utskiftning av aortaklaffen. Sistnevnte ble inkludert som kontroller, uten kjent koronarsykdom. Arterieblod ble tatt ved oppstart av anestesi, og biopsier fra epikardialt og perikardialt fett, samt pre-sternalt subkutant fett, ble tatt før den ekstrakorporale sirkulasjonen startet. Materialet ble så prosessert og frosset ned umiddelbart ved -80°C. Ved å sammenligne de oppnådde resultatene i de koronare fettdepotene med resultater fra subkutant fettvev og de sirkulerende nivåene, vil man kunne si noe om subkutant fettvev og sirkulerende protein reflektere det som skjer i de koronare fettdepotene. Subkutant fettvev og sirkulerende proteiner er mere tilgjengelig materiale, når eventuelt andre populasjoner skal undersøkes.
- For å isolere RNA fra fettvev benyttes RNA isolerings kit beregnet på fettvev. Dette er kjente kommersielle metoder som vi benytter ved vårt forskningslaboratorium. Dette gjelder også metoden for å lage cDNA. For å måle genuttrykket av de aktuelle markørene benytter vi oss av polymerase chain reaction (PCR) og måler genuttrykket relativt til en referanseprøve.
- Hvis studenten ønsker å videreføre oppgaven til et fremtidig doktorgradsprosjekt, vil man kunne implementere en studie av ulike adipokiner som skilles ut ra fettvevet og en eventuell analyse av fibrosemarkører i det samme materialet.
Studentens arbeidsoppgaver
- Skrive en mer fullstendig prosjektbeskrivelse
- Laboratorieanalyser
- Isolere RNA fra fettvev (epikardialt, perikardialt og subkutant)
- Lage cDNA fra isolert RNA. cDNA er en kopi av messenger RNA (mRNA), og er et mål på genuttrykket
- Måle genekspresjon av MMP-9, EMMPRIN og TIMP-1 ved hjelp av PCR
- Måle sirkulerende nivåer av MMP-9, EMMPRIN og TIMP-1 ved hjelp av ELISA (enzyme-linked immunosorbent assay)
- Skrive en vitenskapelig artikkel
Om forskningsmiljøet
Vår forskningsgruppe består pr i dag av 1 professor, forskere/ postdocs, PhD stipendiater og 1 forsk-ningsbioingeniør med mastergrad. Vi har et bredt faglig og inkluderende miljø, og studerer i tillegg til remodelering i fettvev ulike aspekter ved inflammasjonsprosessen, koagulasjonsprosessen ved trombe-dannelse i koronararteriene, aldringsprosessen (telomerer), aktivering av granulocytter (Netose) og aksen tarmflora—koronarsykdom. En student vil få god opplæring i de aktuelle molekylærbiologiske metode-ne, samt statistisk veiledning, og vil inngå i vårt forskerteam og delta på jevnlige forskningsmøter og nasjonale og internasjonale kongresser. Vi samarbeider med klinikere ved Hjertemedisinsk avdeling, og har ulike samarbeidsprosjekter sammen med Institutt for eksperimentell medisinsk forskning (IEMF) og Avdeling for geriatri (Oslo Delirium Research Group), begge OUS, og med Universitetet i Linkõping, Sve-rige. Vårt senter deltar også i ulike forskningsnettverk hvor atrieflimmer inngår. Vi kan tilby et dynamisk og sosialt miljø hvor studenten vil bli godt ivaretatt. Tidligere forskerlinjeprosjekter har vært vellykkede og vi har per i dag to tidligere forskerlinjestudenter som er i ulike sluttfaser av sine doktorgradsarbeid.
Mere info finnes på våre nettsider hos Oslo universitetsykehus HF og Universitetet i Oslo.