Bakgrunn
Den menneskelige organisme ble under evolusjonen kolonisert med en sammensatt blanding av mikroorganismer. De fleste av disse finnes i tykktarmen i form av bakterier og utgjør tarmfloraen, også kalt tarmens mikrobiota. Tarmfloraen består av omtrent like mange bakterier som det er celler i kroppen, og har minst 150 ganger større genom sammenliknet med «verten». Samspillet mellom våre egne celler og mikrobiota er en spennende og ny erkjennelse. Vi er avhengig av tarmbakteriene for utvikling og optimal funksjon av immunforsvaret, karforsyningen, nervesystemet samt for fordøyelse av mat og dannelsen av viktige ernæringsstoffer.
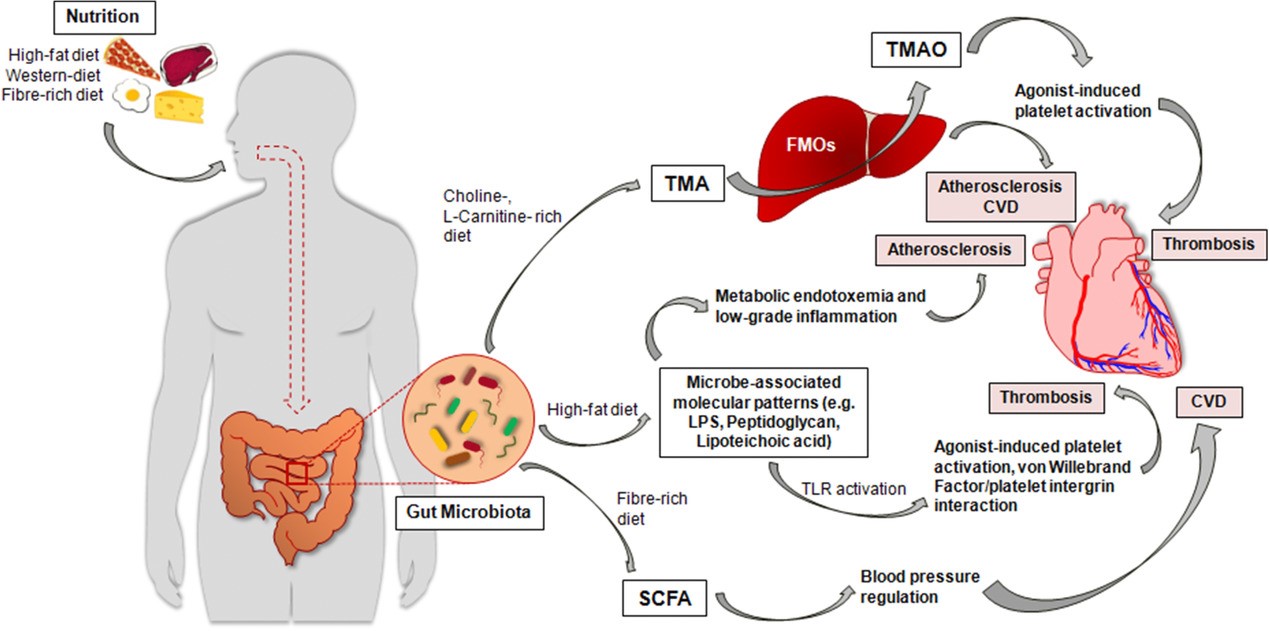
Eur J Immunol, Volume: 48, Issue: 4, Pages: 564-575, First published: 12 December 2017, DOI: (10.1002/eji.201646879
Det kommer stadig ny kunnskap som knytter endring i tarmfloraen til utviklingen av kroniske sykdommer som koronar hjertesykdom, hjertesvikt, fedme og diabetes. En sunn tarmflora kjennetegnes gjerne ved et høyt bakterie-mangfold med individuell stabilitet og funksjonalitet. Tap av dette mangfoldet kalles dysbiose og er et vanlig funn hos personer med ulike sykdommer. Dysbiose kan blant annet føre til en svekket barriere i tarmveggen, som igjen kan føre til at tarmbakterier eller produkter fra tarmbakteriene lettere kan passere tarmveggen og over i blodbanen. Et eksempel er lipopolysakkarider (LPS), et membranmolekyl fra overflaten av gram-negative bakterier. I blodbanen gjenkjennes LPS av immunceller via toll-lignende reseptorer (TLRs). Påfølgende nedstrøms inflammasjonsaktivering kan over tid øke risikoen for utvikling av flere kardiovaskulære tilstander.
Vi kaller en slik lekkasje over tarmveggen for «mikrobiell translokasjon» («gut leakage»). Studier tyder på at gut leakage kan bidra til den kroniske og lavgradige inflammasjonen observert hos noen pasienter med koronar hjertesykdom.
LPS kan også binde seg til toll-lignende reseptor 4 (TLR4) på blodceller og fremprovosere en inflammatorisk respons som trigger aktiveringen av koagulasjonssystemet (Fig. 2), for eksempel ved utslipp av von Willebrand factor (VWF) fra endotelceller og aktivering av leukocytter med påfølgende utslipp av nøytrofile ekstracellulære feller (NETs). Dette kan igjen bidra til akutte trombotiske hendelser som for eksempel et akutt hjerteinfarkt.
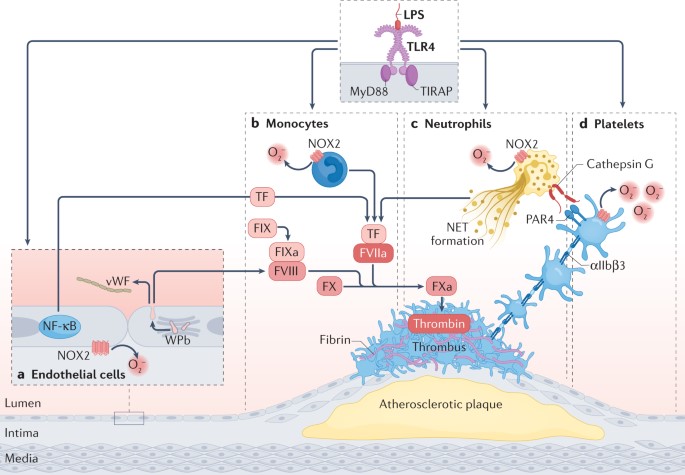
Violi, F., Cammisotto, V., Bartimoccia, S. et al. Gut-derived low-grade endotoxaemia, atherothrombosis and cardiovascular disease. Nat Rev Cardiol 20, 24–37 (2023).
Vi har etablert metoder for å måle lekkasjemarkører som LPS, LPS- bindende protein (LBP), tarm-fettsyre bindende protein (I-FABP) og sCD14 o.a. i serum/plasma. Dette inkluderer både kinetisk kromogen analyse- og ELISA-metoder, samt gen-regulering av disse proteinene med polymerase chain reaction (PCR). Ved å studere disse markørene, ønsker vi å øke forståelsen for tarmfloraens betydning for kronisk, lavgradig inflammasjon og dets rolle som risikofaktor for koronar hjertesykdom og for nye kliniske kardiovaskulære hendelser.
Vi har tidligere vist at høye verdier av LBP gir en økt risiko for å ha metabolsk syndrom og at det er en sammenheng mellom markører for gut leakage (LBP og sCD14) og systemisk inflammasjon ved metabolsk syndrom. I en gruppe eldre menn med økt kardiovaskulær risiko har vi vist at det å ha økte verdier av LBP er assosiert med en økt risiko for nye kardiovaskulære hendelser uavhengig av tradisjonelle risikofaktorer.
Vi ønsker nå å få mer kunnskap om gut-leakage er en underliggende årsak til kardiovaskulære risikofaktorer, koronar hjertesykdom og utviklingen av nye hendelser og død. Videre vil vi undersøke hvordan mikrobiell translokasjon er knyttet til det medfødte immunforsvaret og hyperkoagulabilitet ved akutt koronarsykdom. Det eksisterer lite data fra kliniske studier per i dag.
Problemstillinger
Vi ønsker primært å undersøke hvorvidt:
- Mikrobiell translokasjon (gut-leakage), målt med de sirkulerende markørene LPS, LBP, I-FABP og sCD14 i serum/plasma har sammenheng med kliniske endepunkter (død, nytt hjerteinfarkt, slag, ny revaskularisering og nyoppstått hjertesvikt) (og nyoppstått atrieflimmer) etter 2 år i en populasjon av eldre pasienter med akutt hjerteinfarkt
- Mikrobiell translokasjon (gut-leakage), er assosiert med kliniske karakteristika slik som diabetes, metabolsk syndrom, hypertensjon, og overvekt i samme populasjon
Dette vil inngå i artikkel I
Videre vil vi undersøke om:
- Mikrobiell translokasjon har sammenheng med aktivering av det medfødte immunforsvaret (NETs) og hyperkoagulabilitet (VWF og tissue factor (TF))
Dette vil inngå i en tentativ Artikkel II
Prosjektet vil videre kunne utvides til et doktorgradsarbeid ved å undersøke mangfold i mikrobiota, mikrobiell translokasjon, inflammasjon/ NETs/ hyperkoagulabilitet i andre tilgjengelige populasjoner med koronar hjertesykdom.
Mål og metode
Kliniske data fra en kohort av eldre pasienter med nylig gjennomgått akutt hjerteinfarkt (n= 1027) inkludert etter 2-8 uker), er samlet inn og tilgjengelig i en database (OMEMI-studien). Det samme er kliniske endepunktsdata etter 2 år i samme kohort. En biobank er profesjonelt innsamlet, og plasma/serum er tilgjengelig for dette spesifikke prosjektet.
Mål og hypoteser
- Undersøke sammenhengen mellom mikrobiell translokasjon og kliniske endepunkter etter 2 år. Hypotesen er at markører for mikrobiell translokasjon vil kunne predikere kliniske hendelser
- Beskrive nivåer av mikrobiell translokasjon ved hjelp av nevnte markører i den totale OMEMI-populasjonen og sammenhenger til kliniske karakteristika/ kliniske subgrupper. Hypotesen er at mikrobiell translokasjon (gut leakage) er positivt korrelert til etablerte kardiovaskulære risikofaktorer.
- Utforske sammenhengen mellom mikrobiell translokasjon, NETs og hyperkoagulabilitet i samme populasjon. Hypotesen er at ved gut-leakage frigis inflammasjons mediatorer til blodet som bidrar til økt aktivering av blodceller involvert i kroppens immunforsvar og evne til trombose dannelse.
Metode
Det vil bli gitt opplæring i utførelse av laboratorieanalysene i prosjektet, hovedsakelig ved ELISA-metoder, håndtering av store databaser, samt statistisk veiledning.
Studentens arbeidsoppgaver
Som forskerlinjestudent hos oss vil du få anledning til å:
- Skrive en mer fullstendig prosjektbeskrivelse.
- Utføre laboratorieanalyse av lekkasjemarkører som LPS, LBP, I-FABP and sCD14 og markører for NETs (dsDNA, MPO-DNA og H3Cit) i serum/plasma (med hjelp fra kvalifisert laboratoriepersonell).
- Gjøre statistisk analyse av resultatene i forhold til de problemstillingene som er skissert. Presentere data i tabeller og/eller figurer
- Presentere resultater i forskningsgruppen og ved andre møter/ kongresser
- Skrive 1-2 vitenskapelige artikler som vil kunne inngå i et doktorgradsarbeid
Om forskningsmiljøet
Forskerlinjeprosjektet vil foregå ved Senter for Klinisk Hjerteforskning ved Oslo Universitetssykehus Ullevål.
Velger du å komme til oss, tilbyr vi:
- Et høyt faglig miljø som inkluderer PhD stipendiater, forskere/postdocs, professorer, forskningsbioingeniør og forskningssykepleier/koordinator.
- Vi driver bredt innen klinisk kardiovaskulær translasjonsforskning med interessefelt innen aterosklerose, inflammasjon, tarmflora, koagulasjon/trombose, remodelering, aldring, mm. Miljøet har nasjonale og internasjonale samarbeidspartnere (se link nedenfor)
- En inkluderende og hyggelig arbeidsplass, hvor du som forskerlinjestudent vil bli en naturlig deltaker i vår forskningsgruppe, hvor laboratoriet er en integrert del. Du får delta på jevnlige forsknings-møter og konferanser.
- Målrettet tilrettelegging og veiledning for at ditt forskerlinjeprosjekt skal bli vellykket.
- Det vil være gode muligheter for å utvide prosjektet til å bli et doktorgradsarbeid. Senter for Klinisk Hjerteforskning besitter til dels store biobanker fra større kliniske studier hvor substudier som skissert her er velegnet for forskerlinje- og evt. PhD-prosjekt. Tidligere forskerlinjeprosjekter har vært vellykkede og vi har per i dag to tidligere forskerlinjestudenter som er i ulike sluttfaser av sine doktorgradsarbeid.
Mer informasjon om forskningsgruppen finner du på Senter for klinisk hjerteforskning (SKHF) - Institutt for klinisk medisin (uio.no) og OUH - Clinical Heart Research (ous-research.no)