Hva er presisjonsmedisin og CDSS?
Presisjonsmedisin handler om å skreddersy diagnostikk og behandling for å finne de molekylære årsakene til en sykdom. Når man har funnet disse molekylære årsakene, kan man

gi den enkelte pasient så målrettet behandling som mulig. Det betyr at man ved hjelp av moderne diagnoseverktøy, som for eksempel biomarkører og heleksom- eller helgenomsekvensering, deler pasientpopulasjoner inn i grupper etter om de har nytte av behandlingen eller ikke, eller at man tilpasser behandlingen til den enkelte pasient.
CDSS (cancer drug sensitivity screening, «testing av kreftcellers legemiddelfølsomhet») er én ny metode vi forsker på for å se om vi kan gi klinikere råd om hvordan de kan gi en mer individ-tilpasset kreftbehandling. Det betyr at vi tester et panel av legemidler direkte på kreftceller fra hver pasient in vitro for å se hvilke legemidler som kan drepe kreftcellene fra akkurat den pasienten.
Denne metoden er fortsatt på et tidlig stadium, og den bør brukes i kombinasjon med mutasjonsanalyse og alle andre typer data man har tilgang til fra pasienten. Forutsigelser om hva som vil fungere i pasienter, må også testes i dyremodeller, og det må deretter utføres kliniske studier for å se hvor godt metoden fungerer. Deretter må vi også vurdere hvor stor nytte pasienten faktisk har av dette.
Hvordan arbeider dere med presisjonsmedisin og CDSS ved NCMM/UiO?
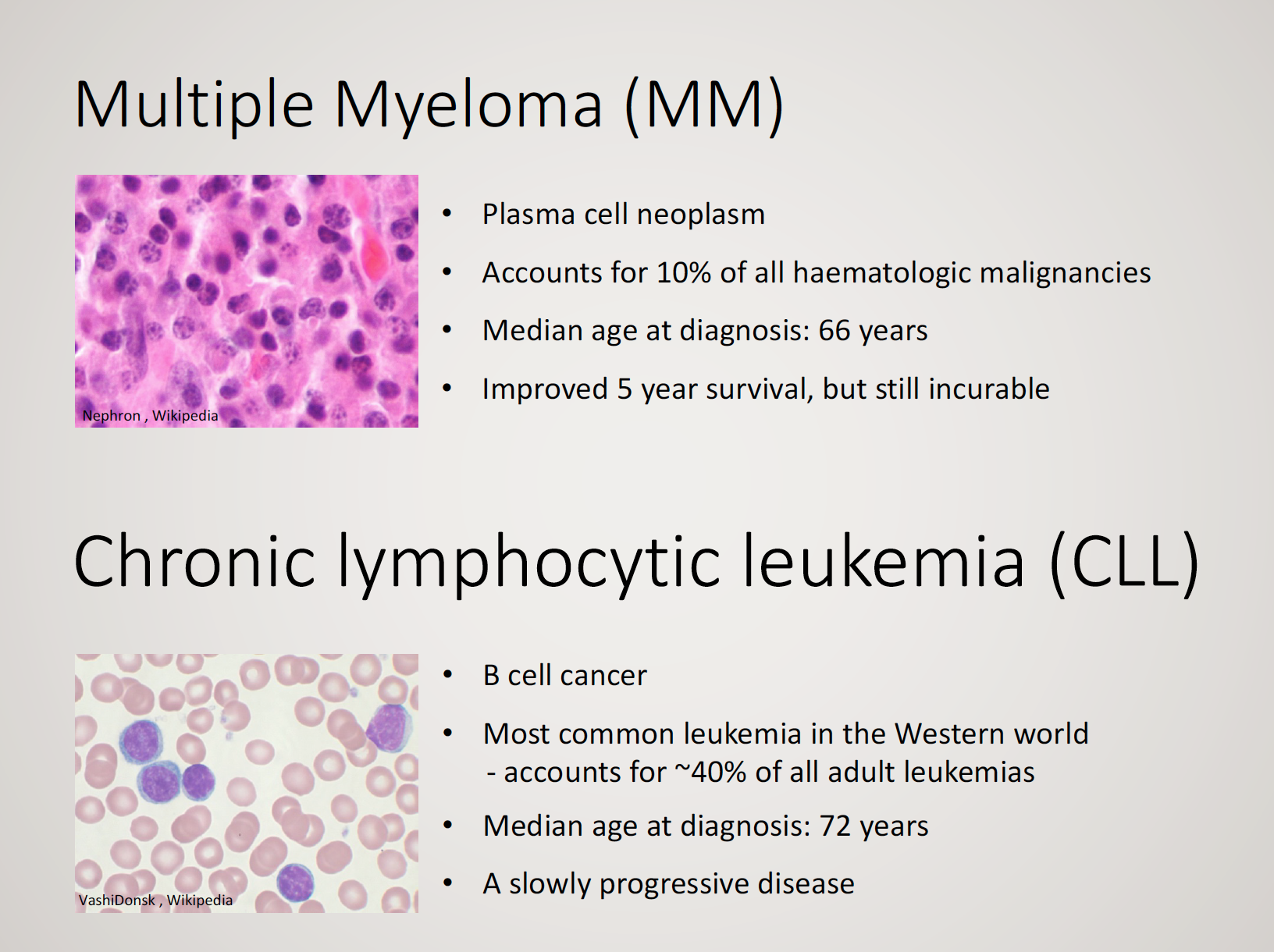
I min gruppe ved NCMM tester vi for tiden rundt 400 legemidler i fem ulike konsentrasjoner mot kreftceller fra pasienter med to typer leukemi – kronisk lymfatisk leukemi (CLL) og myelomatose (MM). Prosjektet er et samarbeid med forskningsgruppene til professor Ludvig Munthe ved Avdeling for immunologi og transfusjonsmedisin ved OUS / Klinmed, UiO, og professor Geir Tjønnfjord og Dr. Fredrik Schjesvold ved Avdeling for blodsykdommer ved OUS, som er finansiert av Helse Sør-Øst RHF og Kreftforeningen. Vårt neste trekk er å modellere med dataene vi har og integrere andre typer informasjon, slik at vi lettere kan forutsi hvilke legemiddelkombinasjoner som kan tenkes å være mer virkningsfulle (forutsi legemiddelsynergi), og teste disse kombinasjonene mot pasientceller.
I siste instans ønsker vi å teste slike forutsigelser i xenograftmodeller med celler som stammer fra pasienter (i samarbeid med gruppene til Dr. Judith Staerk og Camila Esguerra ved NCMM) og deretter i pasienter i små kliniske studier. Vi arbeider nå med å etablere systemets farmakologikomponent for å analysere dataene sammen med Arnoldo Frigessis forskningsgruppe ved Oslo senter for biostatistikk og epidemiologi (OCBE), og også sammen med internasjonale samarbeidspartnere blant annet ved FIMM (Institute for Molecular Medicine Finland) og EMBL (European Molecular Biology Laboratory).
Med konvergensmidlene fra UiO:Livsvitenskap ønsker vi å gå videre med denne tilnærmingen og å se på solide tumorer og, i en mer helhetlig tilnærming der vi har medisinske bildedata, sekvenseringsdata og CDSS-data fra flere svulster i pasienter i og utenfor behandling. Her vil vi utvikle modellerings- og simuleringsaspektene ytterligere.
Hva håper dere å oppdage?
Vi håper å finne metoder for å gi klinikere råd om hvordan de kan tilpasse behandlingen av kreftpasienter som allerede har nyttiggjort seg av andre behandlingsmuligheter. Vi håper å utvikle modeller og algoritmer som gjør at vi kan forutsi, på grunnlag av dataene, hvilke legemiddelkombinasjoner man bør teste, slik at vi sparer pasientmateriale.
Vi håper at vi så vil være i stand til å gå inn i kliniske forsøk for å teste disse forutsigelsene i pasienter og at dette i siste instans gir pasienter en form for utbytte. Jeg håper også at vi vil kunne integrere testing av immunmoduleringsstrategier i CDSS-pipelinen.
Hva tror du disse typene forskning vil bety for kreftbehandling og kreftpasienter i det lange løp?
Jeg tror det er viktig å fortsette å utforske muligheter for pasienter og se på hvilken nytte nye teknologiske framskritt kan gi pasientene. Siden NCMM leder den nasjonale infrastrukturen for kjemisk biologi og høykapasitets screening (NOR-OPENSCREEN) og har en av de fire nodene i dette nettverket, har vi teknologien og robotikken som skal til for å utføre CDSS.
Jeg syntes det var viktig at vi tidlige begynte å arbeide med kreftcellers legemiddelfølsomhet (CDSS) ved NCMM, slik at vi har kompetanse og metoder til å støtte denne type prosjekter. I tillegg til å støtte forskere ved NCMM er det viktig at vi også kan bistå et bredt spekter av slike prosjekter innen ulike krefttyper under ledelse av forskere fra hele Norge.
Hvor håper du at disse behandlingsformene vil være om ti år? Har du flere tanker om framtiden for forskningen innen individtilpasset kreftbehandling?
Når det gjelder CDSS, tror jeg det vil ta rundt fem år før vi har data fra pasienter. Vi må etablere metodene for testing og screening for hver krefttype. Vi vil måtte teste en rekke pasientprøver in vitro, validere funnene i dyremodeller med xeno-transplanterte svulster fra pasienter og deretter teste prediksjoner i de første pasientene i kliniske protokoller.
Hvis vi oppnår gode resultater, vil vi gå videre og teste flere pasienter. Jeg tror det vil ta rundt ytterligere fem år før vi vet hvor stor nytte pasientene har av en slik tilnærming. Jeg tror dette bare er én strategi, og at den vil utvikle seg parallelt med andre metoder. Hvordan veien videre vil bli, er umulig å si i dag. Videre tror jeg at integrasjon av heterogene data, modellering og simulering, og maskinlæring er tilnærminger som sammen i betydelig grad vil kunne få utviklingen til å akselerere. Det skal bli spennende å se hvordan innføringen av slike metoder kan forandre legevitenskapen på mange områder.
.png)