Immunforsvaret består av mange forskjellige celler og proteiner. I tidligere innlegg på Medisinbloggen har du møtt flere av dem. De du oftest hører om er T- og B-cellene og antistoffene. Nå kan du lære litt om en helt annen celletype, makrofagene.
Makrofager har en viktig rolle ved infeksjoner og vevsskade. De er såkalte fagocytter (spiseceller) som spiser innpåslitne mikroorganismer og døde celler. På den måten hjelper de til med å holde vevet ryddig og rent.

Til høyre: makrofager kan strekke ut lange "armer" som fanger opp partikler. (Scanning ektronmikroskopibilde, Wikimedia Commons)
I tillegg har de en rekke funksjoner utover å bidra til immunforsvaret, men som er nødvendig for at vi holder oss friske.
Som ellers i kroppen er det er det viktig med rett balanse, og overaktive makrofager kan bidra til sykdom. Dette ser vi for eksempel ved aterosklerose, fibrose, inflammasjon og kreft. Makrofager er derfor blitt viktige mål når vi utvikler nye terapiformer.
Makrofager tilpasser seg omgivelsene i kroppen
Tidligere trodde vi at makrofagene var relativt uniforme celler som beskyttet kroppen mot infeksiøse agens og ryddet opp etter vevsskade. Ny forskning har vist at makrofager har en rekke ikke-immunologiske funksjoner som er organ-spesifikke.
Makrofagene er meget plastiske celler som kan endre egenskaper ved ytre stimuli, og lokalmiljøet de befinner seg i påvirker funksjonen deres.
For eksempel er det vist at en type makrofager i hjernen – mikroglia – er viktige for å opprettholde et velfungerende nervesystem i hjernen. Det er også vist at mikroglia og makrofager i andre vev kommuniserer med nerveceller. Hjertets makrofager er viktige for hjertets ledningsevne og alveolære makrofager i lungene er viktig for å regulere overflatespenningen i de små blærene (alveolene) der gassutvekslingen skjer.
Nye teknologiske framskritt har gjort det mulig å studere hvilke gener som faktisk er tatt i bruk i hver enkelt celle. Når dette kombineres med avanserte bildeanalyser oppdager vi en videre oppdeling av makrofagene i de ulike vevene. Makrofagene befinner seg i såkalte anatomiske mikro-nisjer og makrofagene i de ulike nisjene har forskjellig funksjon.
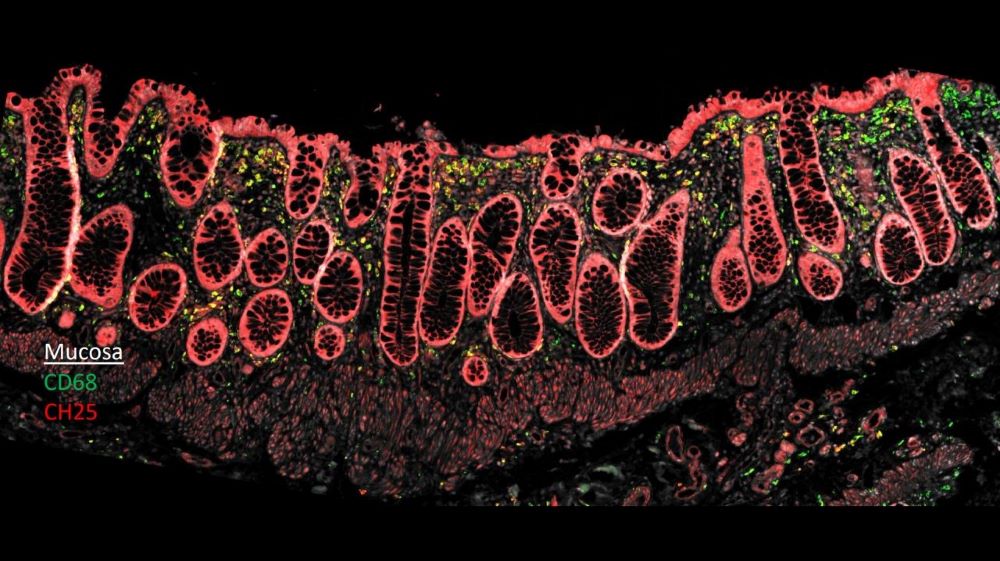
Vår forskningsgruppe studerer makrofager i tarmen. Der ser vi at makrofager som ligger rett under overflaten er effektive på å bryte ned fremmedlegemer og skadede celler. De er også spesielt gode på å stimulere en annen del av immunforsvaret, nemlig T-cellene. Makrofager som ligger langs blodårene, derimot, stimulerer til nyvekst av blodårer mens makrofagene langs nerveceller regulerer nerveimpulser.
Slike nisje-spesifikke egenskaper er vist i flere ulike organer.
Makrofager kan bidra til økt sykdom
Noen ganger «skyter makrofager over mål». Istedenfor å beskytte kroppen mot ytre fare gir de bidrag til sykdomsutvikling.
- Ved skade er makrofager viktig for sårheling, blant annet ved å stimulere celler kalt fibroblaster. Men det kan bli for mye fibroblastaktivitet. Makrofagenes evne til å stimulere fibroblaster synes å være sentralt i det som kalles fibroserende sykdommer, som for eksempel lungefibrose.
- Makrofagene i arterier har vist seg å akkumulere lipider (fettstoffer), og disse lipid-makrofagene kan bidra til aterosklerose/åreforkalkning.
- Ved flere betennelsessykdommer, som for eksempel leddgikt og inflammatorisk tarmsykdom, er det vist at aktiverte makrofager bidrar vesentlig til sykdomsutviklingen.
- Sist men ikke minst er et høyt antall makrofager assosiert med dårlig prognose ved kreftsykdom. Det nok flere årsaker til dette, men det er mulig makrofager oppfatter kreft som et kronisk sår og at de hele tiden prøver å «lege» såret. I den prosessen kan de stimulere til vekst av noen typer kreftceller, de kan bidra til nydannelse av blodårer i svulsten og de kan hemme immunresponser. Dette er prosesser som gir kreftcellene en fordel.
Nye former for terapi sikter seg inn på makrofager
Makrofagenes evne til å endre egenskaper ved ytre stimuli er noe vi forskere ønsker å benytte terapeutisk. Det er for tiden stor forskningsaktivitet med målsetning om å manipulere akkurat makrofagene.
Ved kreft kan en mulighet være å stimulere makrofagene i kreftsvulsten til å aktivere immunapparatet istedenfor å hemme det. Ved kroniske betennelsessykdommer kan målet være å redusere aktivitetsnivået til makrofagene.
Men hvordan kan vi målstyre behandlingen til akkurat makrofager? Dette er mulig ved å bruke små molekyler eller terapeutiske antistoffer som binder seg til spesifikke molekyler på makrofagene. Denne bindingen gir signaler til makrofagene som endrer makrofagenes funksjon i den retning vi ønsker.
Vi ser at slik målstyrt påvirkning av makrofager er en svært spennende strategi for behandling av en rekke ulike sykdommer.